盈飞无限在您身边
业务咨询:
marketing@infinityqs.cn
在线服务:
service@infinityqs.cn
电话:400-812-1268
010-65699909
业务咨询:
marketing@infinityqs.cn
在线服务:
service@infinityqs.cn
电话:400-812-1268
010-65699909
飙升的召回事件
| 作者:Rick Sloop 先生 原文:《 Medical Device Network 》电子杂志 |
|
对于医疗器械制造业来说,质量已成为区分企业优劣的试金石。生产环境的日益复杂,业内公司的频繁兼并,以及跨国供应链资源的复杂利用正导致医疗器械领域的质量问题呈逐步上升趋势。
从安全和经济影响的角度来看,产品品质低劣将带来召回的严重后果。在美国,食品药品管理局(FDA)2008年召回的医疗器械事件的数量达到845件,是1998年358件召回事件数量的两倍多。这一变化是史无前例的。 尽管现在所生产的医疗器械的数量大大超过过去,而且制作过程也更复杂,但出现这样的上升趋势,仍然需要引起人们的警惕(见图1)。 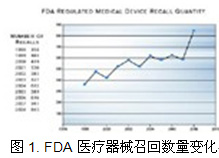 样值得警惕的是在这些召回事件中,有17件属于I类。FDA 所规定的I类产品召回事件是指使用该产品可能严重地损害健康、甚至危机生命。2008年典型的I类召回事件包括:
虽然这里列举的数据都来源于美国 FDA,但是这里提到的医疗器械质量问题却是一个全球性的问题。尤其在社会化生产的今天,制造商往往会从不同的国家采购零部件或原材料,同时他们生产的产品又将销售到不同的国家。要想真正实现对一个过程的监控,唯一的方法就是去了解它在正常统计界限中的表现。” 几乎每个国家或国家联盟都设有管理团体去监控管理生产及进出口。例如,欧盟所有的成员国都必须共同遵循医疗器械管理方面的法律。同时,每个欧盟成员国都有各自独立的与 FDA 行使同样职能的机构来管理医疗器械产品。 虽然这些体系各不相同,但是它们的服务目的是相同的,因此这些体系之间存在许多共通性。例如:许多国家使用ISO-13485:2003标准作为设计和生产医疗器械企业管理系统的基本要求。 ISO-13485:2003的大部分内容主要是针对过程的监控和测量要求。该标准不仅明确了企业在医疗器械行业必须建立和实施监控和测量过程的方法,还应当具备适当的纠错功能,以达到预期效果。 在这其中,如果要以减少生产不合格品的风险为目标,那么最好的方式就是遵循ISO-13485:2003的建议,对生产过程进行监控。而实现对生产过程进行监控的唯一方法就是去了解它在正常统计界限中的表现。一旦发现异常的波动,就可立即按照规则改进过程了解生产过程表现的最佳途径就是统计过程控制(SPC)。因为它不仅能帮助我们很好的掌握正常的生产状态,同时,还能立刻觉察到生产波动。 什么是统计过程控制? SPC 是指利用测量值或数据对生产过程进行控制并改进过程的方法。SPC 数据是在生产过程中实时采集的,并通过对这些数据的分析而实现对过程的监控,因此任何可能会影响最终产品的波动事件都能在生产过程中被检测并改正。相对于其他依靠最终成品检测的事后管理模式,SPC最大的优势之一就是它的预防模式。SPC 数据不仅涵盖了测量值(计量型数据),还包括不合格项数或不合格品数(计数型数据), 因此SPC适用于于所有制造业或服务业过程。 根据 SPC 数据绘制成的控制图定义了过程的正常表现或一般原因波动。如果过程数据在控制限内,那么过程是按照我们希望的方式运作。 如果我们调整一个处于受控状态或所有过程数据都在控制限内的过程,那么我们就是在干预过程。干预一个受控的过程将增加波动和生产不合格品的风险。超过控制限的数据显示过程已有变化,异常原因导致了波动的增加。当一个异常原因发生,应该对它评估并且必须采取行动纠正它(见图2)。 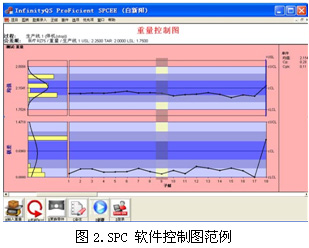 美国统计学家戴明曾经说过“产品质量是生产出来的,不是检验出来的”。SPC是帮助我们使用足够的记录,提前发现问题的工具,它为把质量打造到产品的生产过程中提供了理论基础。 SPC的运用不仅仅是监控整个生产过程的发展,它也会对异常原因引起的波动进行报警,并帮助质量管理人员消除波动,从而改进过程。基于SPC的运用,质量改进的决策将根据生产现场的情况而实时做出,而不是生产出来以后才决定,避免了质量缺陷损失的持续产生。因此运用SPC将大幅度的减少过程的波动,并最终减少报废和返工,提高生产力。运用SPC的另一项益处是SPC要求把关键特性绘制成控制图。这些控制图将揭示过程的“特性”,并通过过程“特性”来突显设备的异常、原材料的问题,甚至是操作员需要培训等。 医疗器械领域中的SPC软件 评估SPC软件系统,首先必须考虑软件能够实时采集过程数据,并且以容易理解、符合统计学原理的控制图形式呈现给用户。软件同样需要包含分析工具,从而帮助用户进行对比分析,揭露潜在的相关性影响,并指导将来的过程改进。 然而,在医疗器械领域中实施SPC软件系统时,必须考虑系统遵循相关行业法律法规。不管其目的是为了满足 CFR 第11章、ISO-13485:2003还是国家法规系统,SPC系统都应该满足以下需求:
除了应具备适当的安全、审核、可追溯特性和实时SPC控制图,一个理想的系统同样要确保符合您的抽样策略。如果没有正确采集数据或证据证明检查工作已经完成,那么即使是世界上最好的统计过程控制系统也几乎是没用的。 “如果没有正确采集数据或证据证明检查工作已经完成,那么即使是世界上最好的统计过程控制系统也几乎是没用的。”如果在考虑满足行业法律法规需求的同时,软件中的动态抽样方案和抽样匹配报告同样也是非常重要的指标。动态抽样方案应该根据过程的状态在准确的测量时间提示操作员抽样。同时,其还应该在过程没有按照要求进行抽样时通知相关负责人。这个特征还应该包括抽样匹配报告,此报告包含指定的范围要求采集多少样本,实际测量了多少样本、抽样比例和其它基本信息,如过程状态、零件和设备信息。例如,如果过程处于正常状态,系统将每30分钟提示操作员抽样;如果过程处于加严抽样状态,系统将每15分钟提示操作员抽样(见图3)。当过程闲置或停止时,停止抽样,并记录停机信息。 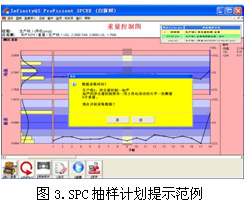 SPC软件还应具备:用于追溯成品组件批次的批次谱系报告;发生过程事件时,可以通过事件监控系统提示采取措施,如发送邮件进行通知,甚至停止过程;包含有抽样检验模块对来料或组件评估。 公司的职责 在评估SPC软件时,软件公司本身的资质也是同样重要的。这个软件公司是否稳定?是否盈利?它在SPC软件行业的排名是多少?它们是否在持续研发产品?他们的团队中是否拥有技术专家、统计学家和经验丰富的技术支持人员,时刻准备为您提供帮助?虽然有上百种SPC软件程序可以创建控制图,但如果您准备创建世界一流的过程控制系统,选择范围是非常有限的。 |